Буферные решения жидкости на водной основе, которые включают в себя как слабую кислоту, так и ее сопряженное основание. Из-за их химического состава буферные растворы могут поддерживать pH (кислотность) на почти постоянном уровне, даже когда происходят химические изменения. Буферные системы встречаются в природе, но они также чрезвычайно полезны в химии.
Использование для буферных решений
В органических системах природные буферные растворы поддерживают рН на постоянном уровне, позволяя протекать биохимическим реакциям без вреда для организма. Когда биологи изучают биологические процессы, они должны поддерживать одинаковый постоянный уровень pH; для этого они использовали подготовленные буферные растворы. Буферные решения были впервые описаны в 1966 году; многие из тех же самых буферов используются сегодня.
Чтобы быть полезными, биологические буферы должны соответствовать нескольким критериям. В частности, они должны быть водорастворимыми, но не растворимыми в органических растворителях. Они не должны проходить через клеточные мембраны. Кроме того, они должны быть нетоксичными, инертными и стабильными во всех экспериментах, для которых они используются.
Буферные растворы встречаются в плазме крови естественным образом, поэтому в крови поддерживается постоянный уровень рН от 7,35 до 7,45. Буферные решения также используются в:
- процессы брожения
- умирающие ткани
- химический анализ
- калибровка измерителей pH
- Выделение ДНК
Что такое Трис-буферное решение?
Трис не хватает трис (гидроксиметил) аминометана, химического соединения, которое часто используется в физиологическом растворе, потому что оно изотоническое и нетоксичное. Поскольку Tris имеет pKa 8,1 и уровень pH от 7 до 9, буферные растворы Tris также широко используются в ряде химических анализов и процедур, включая экстракцию ДНК. Важно знать, что рН в трис-буферном растворе изменяется с температурой раствора.
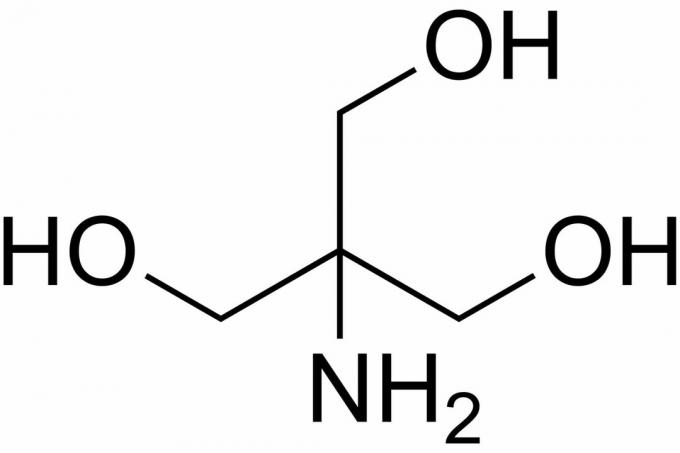
Как приготовить трис-буфер
Легко найти коммерчески доступный трис-буферный раствор, но можно сделать его самостоятельно с соответствующим оборудованием.
материалы:
Рассчитайте количество каждого необходимого вам продукта на основе молярной концентрации раствора, который вы хотите, и количества буфера, которое вам нужно.
- трис (гидроксиметил) аминометан
- дистиллированная деионизированная вода
- HCl
Процедура:
- Начните с определения какой концентрации (молярность) и объем трис-буфера, который вы хотите сделать. Например, буферный раствор Трис, используемый для солевого раствора, варьируется от 10 до 100 мМ. Как только вы определились с тем, что делаете, рассчитайте количество молей Триса, которое требуется, умножив молярную концентрацию буфера на объем буфера, который производится. (моль трис = моль / л х л)
- Затем определите, сколько грамм Триса это, умножив количество молей на молекулярную массу Трис (121,14 г / моль). грамм трис = (моль) х (121,14 г / моль)
- Растворите Трис в дистиллированной деионизированной воде, от 1/3 до 1/2 от желаемого конечного объема.
- Смешать в HCl (например, 1 М HCl) до рН-метр дает вам желаемый рН для вашего буферного раствора Трис.
- Разбавьте буфер водой, чтобы достичь желаемого конечного объема раствора.
После приготовления раствора его можно хранить в течение нескольких месяцев в стерильном месте при комнатной температуре. Длительный срок хранения трис-буферного раствора возможен, потому что раствор не содержит белков.